来源:药脉通
继血脂康后,阿斯利康又将一款国产药纳入麾下。
2月28日,阿斯利康宣布与君实生物宣布一项重磅战略合作,双方将基于各自在药品研发、市场覆盖、渠道拓展等领域的优势资源,积极探索在肿瘤领域的全新深度合作。
自2021年2月28日起,阿斯利康将正式获得君实生物自主研发的抗PD-1单抗药物特瑞普利单抗注射液(拓益)在中国大陆地区非核心市场的推广权,以及后续获批上市的尿路上皮癌适应症的全国独家推广权,君实生物将继续负责拓益在中国大陆地区除尿路上皮癌之外获批适应症的核心市场推广。
药脉通副总王鹏表示,阿斯利康的代理之路终于找对了。
2019年6月,阿斯利康召开誓师大会,号称要开启非凡征程,誓将阿斯利康打造成中国最伟大医药公司,年销售额要达到150亿美金,折合人民比近千亿。仅仅依靠阿斯利康本身产品,要实现年销售额过千亿人民币的目标并不容易,阿斯利康还需要不断找产品。

血脂康是阿斯利康找到第一个备受关注的产品,但是,用学术推广、学术教育的方法做推广,本身适合高知识维度的产品进行学术传递和学术教育,从医生检查、诊疗、诊断、推广规范化去做,血脂康并不有利于发挥阿斯利康的这个优势。后来阿斯利康也代理过一些医疗器械类产品等,并不能带来很大市场销售。而PD-1、PD-L1是肿瘤治疗划时代的产品,有千亿市场空间,能够很好地发挥阿斯利康的优势。肿瘤产品迭代很快,可以想见,拓益不会是阿斯利康代理的最后一个产品,只能算是一个良好开端。
阿斯利康本身亦有PD-1产品,缘何还与君实生物合作?
近日,阿斯利康宣布,主动撤回旗下的PD-L1(英飞凡)在美国市场用于既往接受过治疗的成人局部晚期或转移性膀胱癌的适应证,其原因在于未能满足美国FDA对新药上市后再评价的要求。该药的适应症扩大遭遇挫折,公开资料显示,英飞凡在中国内地获批 lll期非小细胞肺癌维持治疗适应症。
相比较英飞凡,拓益是国内首个上市国产PD-1药物,获批的第一个适应症为黑色素瘤的治疗。今年2月,拓益获批可用于鼻咽癌患者的治疗,是全球首个获批鼻咽癌治疗的PD-1单抗药物。此外,拓益适用于既往接受系统治疗失败或不可耐受的局部进展或转移性尿路上皮癌患者的治疗的新适应症上市申请获得NMPA受理,并在2020年7月被NMPA纳入优先审评程序。显然,虽然同为PD-1药物,但二者在适应症上并不冲突。
行业人士表示,肿瘤药物是阿斯利康的主战场之一,但英飞凡非一线、二线用药,只是维持治疗,扩大适应症的冲击又失利,君实生物拓益的代理权显然有利于巩固、扩大阿斯利康在肿瘤领域的优势。
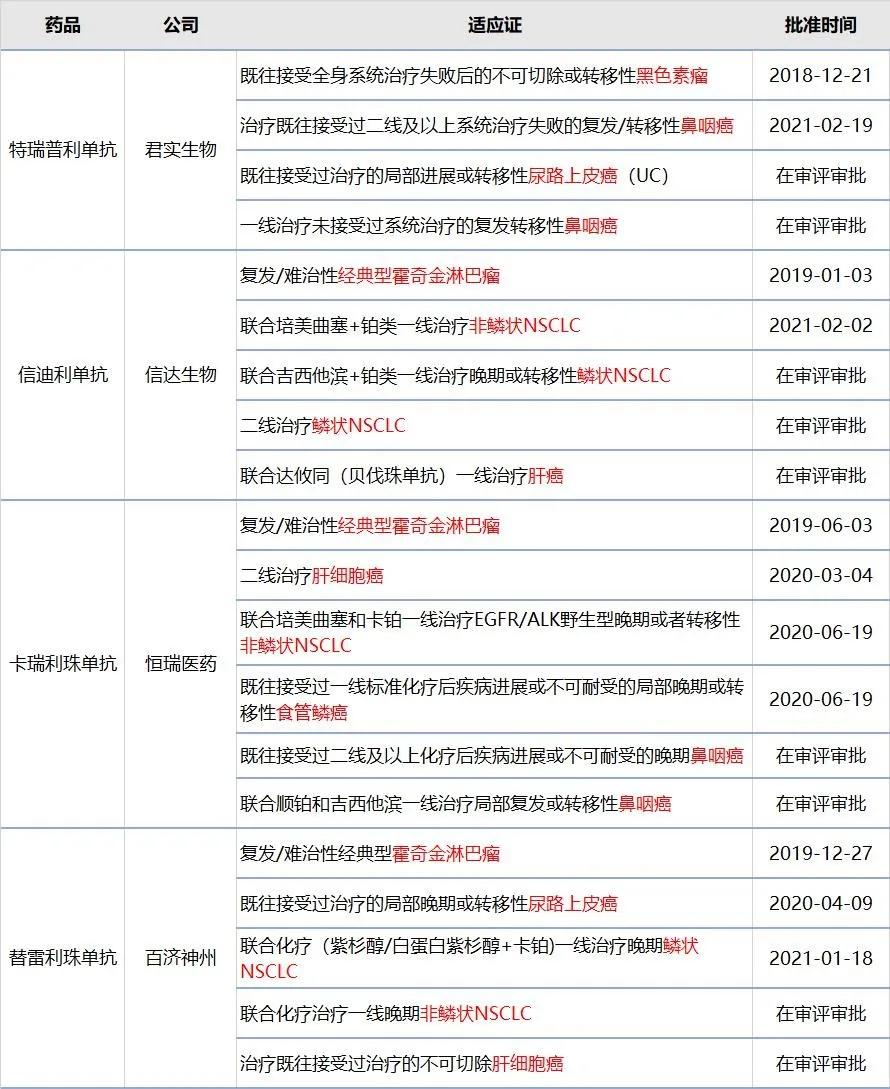
图片来源:医药魔方
君实选择和阿斯利康合作和PD-1背后激烈的市场竞争分不开。
作为国产PD-1,君实生物的拓益于2018年底最先上市,但是,随即信达生物的信迪利单抗(达伯舒)上市,并在2019年的国家医保谈判中,达伯舒谈判成功被纳入医保,君实生物选择了放弃。其实,君实生物的解释是,目前PD-1适应症比较单一,未来随着适应症范围的扩大以及剂量规格多样化的实现,君实会以更加积极的姿态申请加入医保。
受益于医保谈判准入,达伯舒销售额后来居上,日前,信达生物发布预告称2020年销售额超过22亿元,而据君实生物发布2020年业绩快报,营业总收入15.95亿元,主要来自于拓益的销售收入。
信达并不算是拓益最强势的追兵。
百济神州的替雷利珠单抗(百泽安)于2020年3月在中国获批上市,但是,有辉瑞中国前老大吴晓滨掌舵,百济神州近日披露的年报显示,刚刚上市不到一年,百泽安就卖了11个亿。
此外,还有恒瑞的卡瑞利珠单抗(艾瑞卡),该产品于2019年5月上市,坊间传闻在2020年前三季度,其销售就已经突破了30亿。
2020年底,国家新一轮医保谈判结果公布:百济神州、君实和恒瑞三家企业的PD-1产品成功入围,加之2019年谈判成功的信达生物,4款国产PD-1被纳入医保目录,产品力、销售力成为竞争核心。
王鹏表示,君实生物目前PD-1只有400多个人队伍,未来PD-1下县域、基层也是趋势所在,阿斯利康本身有强大销售队伍,急于扩大市场君实和急需好产品的阿斯利康的合作显然是意料之中。
版权声明:我们致力于保护作者版权,注重分享,被刊用文章【药品代理商(阿斯利康)】因无法核实真实出处,未能及时与作者取得联系,或有版权异议的,请联系管理员,我们会立即处理! 部分文章是来自自研大数据AI进行生成,内容摘自(百度百科,百度知道,头条百科,中国民法典,刑法,牛津词典,新华词典,汉语词典,国家院校,科普平台)等数据,内容仅供学习参考,不准确地方联系删除处理!;

工作时间:8:00-18:00
客服电话
电子邮件
beimuxi@protonmail.com
扫码二维码
获取最新动态
